NADHについて
細胞内でNADとNADHのバランスが崩れることは、細胞の代謝状態や健康状態に大きな影響を与える可能性があります。以下のような状態を示すことがあります:
酸化ストレス:
- NADHが過剰になると、酸化還元バランスが崩れ、酸化ストレスが増加します。これにより、細胞損傷や炎症が引き起こされることがあります。
エネルギー代謝の異常:
- NADが不足すると、ATPの生成が減少し、エネルギー不足を引き起こします。これは、疲労感や筋力低下などの症状を引き起こす可能性があります。
代謝疾患:
- NAD/NADHバランスの異常は、糖尿病や肥満、心血管疾患などの代謝疾患と関連しています。
老化:
- NADレベルの低下は、老化プロセスと関連しており、細胞の修復能力や再生能力の低下を引き起こすことがあります。
ミトコンドリア機能障害:
- NADHが過剰になると、ミトコンドリアの機能が低下し、エネルギー生産が効率的に行われなくなります。
これらの状態は、細胞の健康や全身の健康に深刻な影響を与える可能性があるため、NADとNADHのバランスを維持することが重要です。
ニコチンアミドアデニンジヌクレオチド (英: nicotinamide adenine dinucleotide) とは、全ての真核生物と多くの古細菌、真正細菌で用いられる電子伝達体である。さまざまな脱水素酵素の補酵素として機能し、酸化型 (NAD+) および還元型 (NADH) の2つの状態を取り得る。二電子還元を受けるが、中間型は生じない。略号であるNAD+(あるいはNADでも同じ)のほうが論文や口頭でも良く使用されている。またNADH2とする人もいるが間違いではない。
かつては、ジホスホピリジンヌクレオチド (DPN)、補酵素I、コエンザイムI、コデヒドロゲナーゼIなどと呼ばれていたが、NAD+に統一されている。別名、ニコチン酸アミドアデニンジヌクレオチドなど。
構造と物理化学的特性
NAD+はニコチンアミドモノヌクレオチドおよびアデノシンからなる物質であり、ヌクレオチドの5'がそれぞれリン酸結合によって結合している構造を取る。アデノシンの2'には-OH基が付属しており、これがリン酸基に置換されると、NADP+となる。
酸化還元反応に関与しているのは、ニコチンアミドであり、酸化型および還元型の構造は図の通りである。(還元型は4位の炭素に立体特異性がみられる。)

上図では、水素原子が1つだけ付加されたように見えるが、ニコチンアミドのN+が電子によって還元されるために、結果として2つの水素原子を運搬しているのと同じ状態となる。すなわち、全体としての二電子酸化還元反応は以下の通りである。
- NAD+ 還元物質 (2e−+2H+)⟷NADH+H++ 酸化物質
酸化還元電位 (Eo') は-0.32Vである。
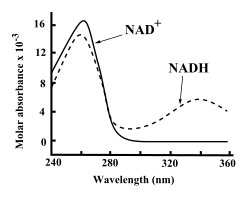
アデニン塩基を含むことから、NAD+とNADHはともに強いUV吸収を示す。NAD+の吸収ピークは259 nmで、モル吸光係数は16,900 M−1cm−1である。一方、還元型のNADHのみ、339 nmに第2の吸収ピークを持ち、そのモル吸光係数は6,220 M−1cm−1である。この第2のピークは酸化型のNAD+には存在しないため、分光光度計を用い波長340nmあるいは339nmの吸光度を測定することでNAD+とNADHの間の酸化還元反応を簡単に測定することができる。[1]脱水素酵素活性測定にはこの方法が良く用いられている。
NAD+とNADHは蛍光にも差が存在している。水溶液中のNADHは460 nmをピークとする寿命0.4 nsの蛍光を発するが、NAD+は蛍光を発しない。[2]NADHの蛍光特性はタンパク質に結合すると変化するため、これを用いて解離定数を測定することができる。[2][3]また蛍光顕微鏡を使って生細胞の酸化還元状態を測定することも可能である。[4]
ヒトの肝細胞内でNADHが合成される反応は多岐にわたりますが、以下に代表的な反応をいくつか挙げます:
- 解糖系:
- グリセルアルデヒド-3-リン酸デヒドロゲナーゼ反応
- ピルビン酸デヒドロゲナーゼ複合体:
- ピルビン酸からアセチルCoAへの変換
- クエン酸回路(TCA回路):
- イソクエン酸デヒドロゲナーゼ反応
- α-ケトグルタル酸デヒドロゲナーゼ反応
- マレートデヒドロゲナーゼ反応
- 脂肪酸β酸化:
- アシルCoAデヒドロゲナーゼ反応
- アルコール代謝:
- アルコールデヒドロゲナーゼ反応
- アルデヒドデヒドロゲナーゼ反応
これらの反応は、肝細胞内のミトコンドリアや細胞質で行われ、エネルギー代謝や解毒作用に重要な役割を果たしています
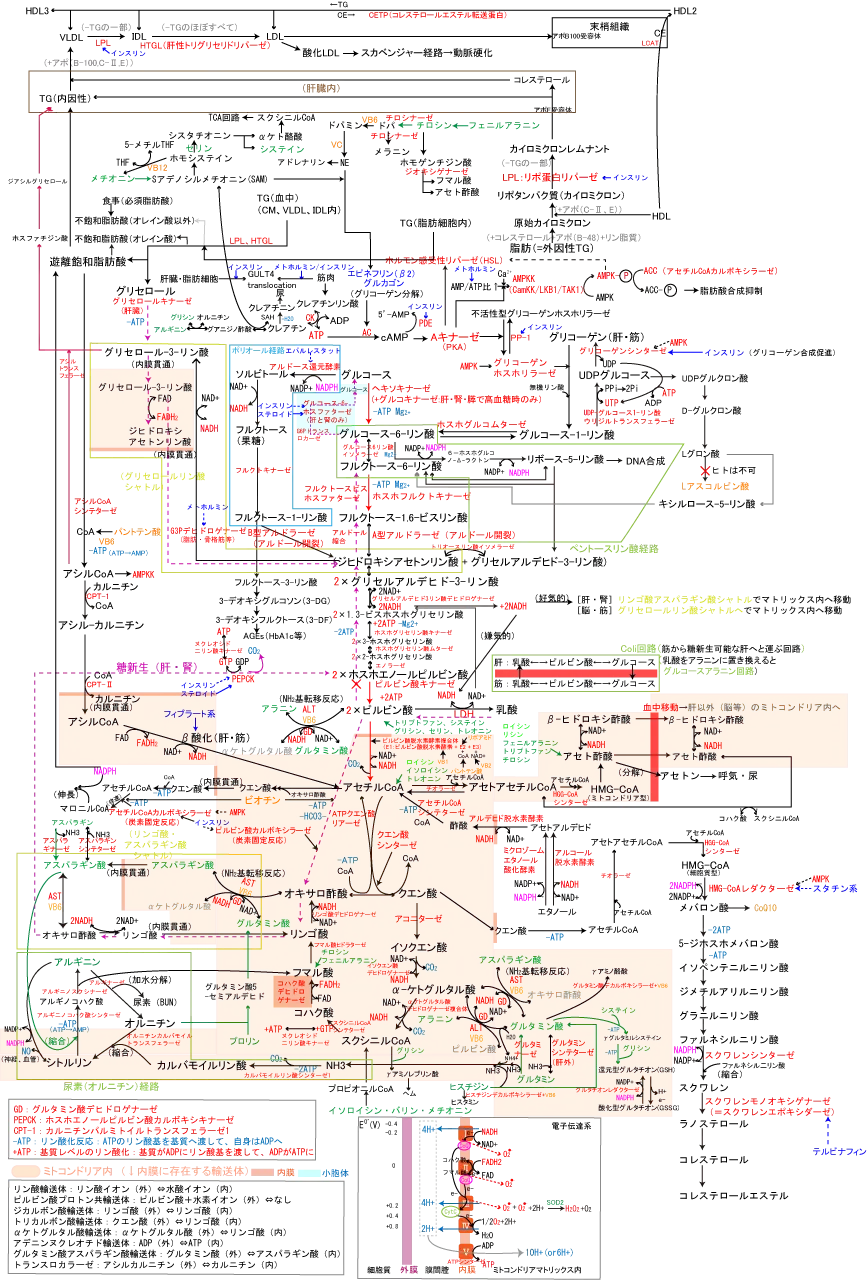
- グルコース1モルからのATPとNADH、FADHの収支。括弧内は赤血球で迂回路に入りホスホグリセリン酸キナーゼの反応がスキップされた場合。
1molのNADHは10H+の勾配を作り、4H+の勾配が1ATPであるので2.5molのATPを生成する。1molのFADH2は6H+の勾配を作るので1.5molのATPを生成する。使用 生成 収支 解糖系 2ATP 4(0)ATP
2NADH2(0)ATP
2NADH(=5ATP)PDH なし 2NADH 2NADH(=5ATP) TCA回路 なし 2GTP(=ATP)
6NADH
2FADH22ATP
6NADH(=15ATP)
2FADH2(=3ATP)合計 - - 32(30)ATP - ATP(アデノシン三リン酸)、ADP(アデノシン二リン酸)、NAD+(ニコチンアミドアデニンジヌクレオチド)、NADH(還元型ニコチンアミドアデニンジヌクレオチド)、FAD(フラビンアデニンジヌクレオチド)、FADH2(還元型フラビンアデニンジヌクレオチド)
- 1molのグルコースは分子量180なので約180g/mol、1molのグルコースにはアボガドロ数の分子が含まれる、1gのグルコースは(1/180)mol。グルコース1分子は(1/アボガドロ数)molであり、(180/アボガドロ数)グラム。
- グルコース1分子から得られるATP:約30~32分子のATP
- グルコース1molから得られるATP:約30~32molのATP。1molのグルコースは、アボガドロ数(約6.022×10^ 23)のグルコース分子を含んでいて30~32molのATPは、(30~32)×6.022×10^23分子のATP。
- グルコース1gから得られるATP:30~32/180molのATP。ATPのモル質量が507.18g/molなので、約84~90 gのATPが生成
- 1カロリー (cal) は、4.184ジュール (J) に等しい。グルコース1g=4kカロリーは16736ジュールに等しい。
- ATPの1molが加水分解されてADPになる際に放出されるエネルギーは、約30kJ/mol(=30/4.184=7.3kcal/mol)。32molのATPで約960kJ(229.4kcal)。1molのグルコースの完全酸化によって放出されるエネルギーは約686kcal/molで、このうちATPとして取り出せるのは229.4kcalで残りの約450kcalはATPの合成以外で使われたエネルギー(熱、他の代謝経路、エネルギー損失等)。
つまり、1gのグルコースを完全酸化させて水と二酸化炭素になった場合のエネルギーは約4kcalだが、1gのグルコースから作られるATPは約1.5kcalである。それもこれはATP→ADPで計算したものでATP→AMPであればさらにエネルギー量が多くなる。残りは他で使われるか蓄えられるかされたエネルギーである。 - 還元剤とは電子を与えて自分が酸化されるもの、酸化剤とは電子を受け取って自分は還元されるもの。
- NAD+は2つの電子(及び1プロトン)を受け取って自分が還元されるので酸化剤として働き、NADHは2つの電子(及び1プロトン)を与えて酸化されてNAD+とH+になる(NADH→NAD++2e-+H+)ので還元剤である。なお、NADH2+の表記はNADHの分子が2つの正の電荷をもつカチオンであることを示す形であり、NADH+H+と同じ意味(ここのH+はNADHが酸化されてNAD+に戻るときに放出されるプロトンを示す。ただわかりにくいので現在はNADHとの記載が主流)。
- ATPを使わない酵素をシンターゼ synthase、使う酵素をシンテターゼ synthetase と呼ぶ
- ATPが基質をリン酸化してADPになることは単にリン酸化反応の一つ、逆にADPが基質によりリン酸化されてATPになることを基質レベルのリン酸化と呼んでいる。
- ミトコンドリア内膜通過:ATP、ADP、ピルビン酸、クエン酸、αケトグルタル酸、リンゴ酸、グルタミン酸、アスパラギン酸
- ミトコンドリア内膜通過できない:NADH、アセチルCoA、アシルCoA、オキサロ酢酸
- 血液中を移動可能な物質:乳酸、ケトン体、グルコース、アミノ酸、脂肪酸、ビタミンとミネラル、コレステロールとリポたんぱく質、尿素、ホルモン、電解質等
- ケトン体・・・アセト酢酸、βヒドロキシ酢酸、アセトンの総称
- 活性酸素(Reactive Oxygen Species, ROS)・・・スーパーオキシドアニオン、過酸化水素、ヒドロキシラジカル、一酸化窒素、ペルオキシニトリート、シングレット酸素等
- 活性酸素の作用・・・強力な酸化剤。他の分子(脂質、タンパク質等)から電子を引き抜く(酸化する)ことができる。活性酸素は電子が1つ過剰なので電子を与えるかと思いきや生物学的な環境下では引き抜く作用の方が強いため酸化剤としてふるまう。これに対して、ビタミンEやC、グルタチオン等の抗酸化物質はラジカルスカベンジャーとしてフリーラジカルを中和する作用がある。
- シャトル経路・・・内膜を通過できないNADHをミトコンドリア内にあたかも運んでいるように見せる経路。
- リパーゼ・・・脂肪を分解して脂肪酸とグリセロールに分解する酵素で大きく3つある。
- 膵リパーゼ:膵臓から分泌されて、小腸内で食物中のトリグリセリドを加水分解する。
- リポタンパク質リパーゼ:血液中に存在するキロミクロンやVLDLなどリポタンパク質のトリグリセリドを加水分解する
- ホルモン感受性リパーゼ:白色脂肪細胞内に蓄積されているトリグリセリドを加水分解する。
- 赤血球はミトコンドリアを持たない。脂肪細胞のうち脂肪をため込むだけの白色脂肪細胞もミトコンドリアがほとんどない。
- αケト酸とはカルボキシル基とケトン基を持つ有機化合物のことで、代表的なものがピルビン酸、αケトグルタル酸、オキサロ酢酸の3つ。
- HMG-CoAにはミトコンドリア型と細胞質型の2つがある。ミトコンドリア型はケトン体の合成に、細胞質型はコレステロールの合成に必要である。
- ΔGは自由エネルギーの変化
肥満・高血糖・脂質がミトコンドリアに与える影響
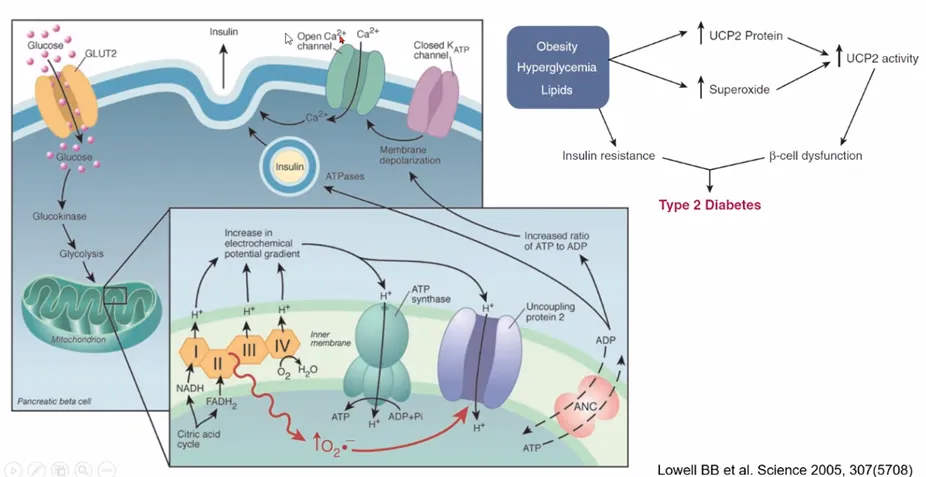
肥満や高血糖はUCP2蛋白やスーパーオキシドを増加させると言われる。
UCP(uncoupling protein:脱共役蛋白)は、ミトコンドリアでの電子伝達系とATP合成が膜でのプロトン濃度勾配によって密に共役しているのに対して、この共役を短絡的に解消する特殊なチャネルであり、これが活性化されると、酸化基質の化学エネルギーはATP合成に利用されずに、熱へと変換される。(ミトコンドリア共役蛋白質UCPファミリーとエネルギー消費・肥満より)
肥満状態等でなければ、ミトコンドリア内膜上ではプロトン勾配を利用するチャネルのみが動くけど、肥満状態になると内膜上にUCP2タンパクの発現が増え、H+の行き先が分散され、ATPへの変換効率(すなわちインスリン分泌能)が落ちるとされる。
2024年12月11日 | カテゴリー:自然科学的基礎知識//物理学、統計学、有機化学、数学、英語, 生活習慣病 |