HTLV-1(ヒトT細胞白血病ウイルス1型)について
HTLV-1とはなんですか
HTLV-1は、血液中の白血球の一つであるリンパ球のうちのT細胞に感染します。HTLV-1感染細胞では染色体(ゲノム)DNAにウイルス遺伝子が組み込まれ、プロウイルスとして感染細胞中に定着します。B型肝炎ウイルスなどとは異なり、血漿中にはほとんど存在しません。
- HTLV-1の感染は、ウイルスに感染した細胞が対象の体内に入り込むことで成立します。そのため、現在は母乳による保育や性交渉が感染の原因になることが多いと考えられています。以前は輸血を介した感染もありましたが、日本では、昭和61(1986)年以降は日本赤十字社において、献血された血液がHTLV-1に感染しているかを調べるようになったため、現在は国内での輸血による感染はありません。
- HTLV-1が発見されたのは1980年と比較的最近ですが、元々はこのウイルスの原型のウイルス(STLV)がアフリカ大陸のサル属に広く感染しており、それが人類に感染してヒト型のウイルス=HTLV-1となり人類の移動に伴って世界に広がったものと考えられております。その後、人類の移動に伴って世界中に広がり、我が国では縄文時代以前にはすでに日本人に感染していたことが明らかになっており、太古より現代まで日本人に連綿として引き継がれてきたウイルスです。
HTLV-1は体の中のどこに感染していますか血液は、赤血球、白血球、血小板といった細胞の成分と、血漿とよばれる液体の成分から成り立っています。このうち白血球は、体内に侵入した細菌やウイルスなどを攻撃する免疫という機能を担う血球で、好中球、好酸球、好塩基球、単球、リンパ球などに分けられます。リンパ球はさらにT細胞、B細胞、NK細胞などに分類され、HTLV-1はこのうち主にT細胞に感染しています。
HTLV-1はT細胞に入ったあと、どうなりますかT細胞の中に入り込んだウイルスは、ウイルス粒子の殻の中に持っていた逆転写酵素を用いて遺伝子の本体であるRNAをDNAに変換し(この過程を逆転写といいます)、この変換されたDNAがT細胞の染色体(ゲノム)DNAに組み込まれプロウイルスとなります。このように宿主細胞の染色体(ゲノム)DNAにウイルスが組み込まれている状態のことをHTLV-1に感染している(HTLV-1感染者)といいます。HTLV-1感染細胞とはなんですかウイルスが宿主細胞の染色体(ゲノム)DNAに組み込まれた細胞のことを、HTLV-1感染細胞といいます。HTLV-1感染細胞は主にT細胞であるため、ふだんは血液の中やリンパ節などのリンパ組織に存在しています。一度HTLV-1に感染するとずっと感染したままですかHTLV-1の感染は、ウイルスの遺伝子が宿主細胞の染色体(ゲノム)DNAに組み込まれたプロウイルスになることによって起こります。一度組み込まれたプロウイルスは、二度と抜け落ちることなく、その細胞の中で受け継がれていきます。現在のところ、薬などでプロウイルスを排除することはできませんので、一度HTLV-1の感染が成立すると生涯にわたり感染したままとなります。HTLV-1は体の中でどのように感染をひろげますかHTLV-1が感染をひろげる方法は2つあります。1つ目は、HTLV-1に感染していない細胞と接触するとウイルス粒子を渡し、HTLV-1に感染していなかった細胞を感染させることで、感染をひろげる方法です。このような感染方法を細胞間感染とよびます。2つ目は、HTLV-1が感染している細胞そのものを増やして自己の遺伝子のコピー数を増やすもので、これをクローナルな増殖とよびます。体の中でHTLV-1の感染をどのように抑えていますか人は免疫の力によって、ウイルスの感染拡大を防ぐように働きます。したがって、体の中のHTLV-1感染細胞の数は、通常、HTLV-1が感染を広げようとする力と、体がもともと持つ免疫の力とのバランスで一定に保たれています。HTLV-1のプロウイルス量や感染細胞率とはなんですか体の中にどれくらいのウイルスが存在するかを数字で表したものを「プロウイルス量」と呼びます。HTLV-1の場合は、血漿中にウイルス粒子を検出することができないため、ウイルスに感染している細胞の数をウイルス量として表しています。HTLV-1は、感染すると細胞のゲノム(DNA)に「プロウイルス」として組み込まれます。基本的に1個の感染細胞に組み込まれているプロウイルスは一つなので、「プロウイルスの数=感染細胞の数」となります。そのため血液中に感染細胞がどのくらい存在するのかは、測定する全ての細胞の中にいくつのプロウイルスがあるかを調べることでわかります。一般的に血液の単核球(リンパ球と単球)中に含まれるプロウイルス(HTLV-1遺伝子)の数を測定したものをプロウイルス量や感染細胞率といい、単核球100個あたりのプロウイルスのコピー数(コピー/100細胞)や感染細胞の比率(%)として表現します。HTLV-1キャリアとはなんですかインフルエンザウイルスなどとは違って、HTLV-1の場合は感染していても特に症状はありません。HTLV-1感染者の約95%は、生涯にわたりHTLV-1感染が原因となって起こる病気を発症せず、感染していない人と同じように生活することができます。無症状のままHTLV-1というウイルスを持続的に保有している人のことを「HTLV-1キャリア」とよびます。
一方で、HTLV-1キャリアの一部の人は、成人T細胞白血病・リンパ腫(ATL)、HTLV-1関連脊髄症(HAM)、HTLV-1ぶどう膜炎(HU/HAU)などの病気を発症します。HTLV-1に感染するとどのような病気になりますかHTLV-1キャリアは、生涯のうちに約5%の頻度で成人T細胞白血病・リンパ腫(ATL)とよばれる血液の病気を、約0.3%の頻度でHTLV-1関連脊髄症(HAM)とよばれる神経の病気を発症します。また、HTLV-1キャリア10万人あたり90~110人がHTLV-1関連ぶどう膜炎(HU/HAU)という眼の病気を有していることが知られています。その他、シェーグレン症候群、筋炎、肺病変、関節炎などとの関連が疑われていますがその因果関係ははっきりしていません。また、一人の人がこれらの病気を合併して発症することもあります。どのようなHTLV-1キャリアがATLを発症しやすいですか体の中のHTLV-1感染細胞の数(プロウイルス量)は、通常、HTLV-1が感染を広げようとする力と、体がもともと持つ免疫の力とのバランスで一定に保たれています。
しかしながら、何かのきっかけでHTLV-1感染細胞のゲノムに変異などが起こると、HTLV-1感染細胞は自発的に増殖するようになります。このように自発的に増殖するようになった細胞(クローナルな細胞といいます)は「がん化」しやすく、さらにゲノムの変異が蓄積してHTLV-1感染細胞ががん化した状態になるとATLを発症します。そのためクローナルな細胞が増えてきている場合は、ATLを発症するリスクが高いと考えられています。これまでの研究で感染細胞の割合が単核球(リンパ球と単球)の4%以上の方々がATLを発症する危険が高いと報告されています。ゲノムに変異を引き起こすよく知られた原因としては喫煙が知られていますが、HTLV-1キャリアでも、喫煙者にATL発症リスクが高いことが知られています。また、家系内にATLを発症した方がいる場合もATLの発症リスクが高いことがわかっています。どのようなHTLV-1キャリアがHAMを発症しやすいですかHAM患者ではHTLV-1キャリアに比べるとHTLV-1感染細胞の数(プロウイルス量)が多いので、HTLV-1感染細胞数が高いHTLV-1キャリアは、HAMの発症リスクが高いといわれています。HTLV-1感染細胞の増え方には、一つの感染細胞が増えるモノクローナルな増殖と、様々な感染細胞が増えるポリクローナルな増殖といった2つの様式がありますが、HAMの発症リスクが高いキャリアは、ポリクローナルな増殖をしている特徴があります。
またHAMは、免疫が活性化しているという特徴があります。免疫は本来、体の中に外敵が侵入してきた際に攻撃してくれる重要な役割を果たしていますが、その機能が暴走(活性化)しすぎると自分の体を攻撃してしまうことがあります。この免疫の機能を決定する要因として、白血球の型(HLA:Human Leukocyte Antigen)が重要であることはよく知られていますが、特定の白血球の型を保有しているHTLV-1キャリアはHAMの発症リスクが高いことが知られています。
その他にも、腎臓移植などの臓器移植でHTLV-1に初めて感染すると、移植後に数年でHAMを高率に発症するリスクがあることが分かっています。そのため、腎臓移植の際は臓器を提供する方(ドナー)と臓器の提供を受ける方(レシピエント)のHTLV-1抗体検査を移植前に実施し、HTLV-1感染ドナーから非感染レシピエントへの移植は、原則実施しないように推奨されています。どのようなHTLV-1キャリアがぶどう膜炎(HU/HAU)を発症しやすいですかHTLV-1関連ぶどう膜炎(HU/HAU)の患者ではキャリアに比べるとHTLV-1感染細胞の数(プロウイルス量)が多いので、HTLV-1感染細胞数が高いHTLV-1キャリアは、HU/HAUの発症リスクが高いといわれています。
また重要なことに、HTLV-1キャリアがバセドウ病(甲状腺機能亢進症)を発症して、チアマゾール(商品名:メルカゾール)の治療を受けた後に、HU/HAUを発症するリスクが高いことが知られています。いつHTLV-1に感染したかを知ることはできますかHTLV-1に感染しても感染直後に特徴的な症状が現れることはありませんので、定期的にHTLV-1の抗体検査をしない限り、いつ感染したのかを知るのは困難です。HTLV-1キャリアはどのくらいいますか平成21年の厚生労働省科学研究班(山口班)の全国調査によると、HTLV-1 の感染者(キャリア)数は約 108 万人以上と推定されています。また平成26年の日本医療研究開発機構(AMED)研究班(浜口班)の調査では、約72~82万人と推定されています。つまり国民の約100~150人に1人はHTLV-1キャリアであると推定されています。HTLV-1キャリアが多い地域はどこですかもともと九州・沖縄地方に多く、西高東低であることが知られていましたが、近年では人口の大都市圏への移動、集中にともなって大都市圏で増加傾向にあります。日本以外では、カリブ海沿岸、中南米、アフリカなどに多く、最近ではオーストラリアの先住民族にも多いことが明らかになりました。HTLV-1総合対策とはなんですか
HTLV-1総合対策 全文(PDF:175KB)、骨子(PDF:184KB)
HTLV-1対策推進協議会とはなんですか厚生労働省において開催される協議会のことで、HTLV-1 対策に携わる行政、専門家、患者等が参加してHTLV-1総合対策の推進について協議します。HTLV-1母子感染対策協議会とはなんですかHTLV-1 母子感染予防対策を検討するための協議会のことで、国が各都道府県に設置を求めています。厚生労働省科学研究班(板橋班)が実施したアンケート調査では、2017年11月時点で全国47都道府県のうちHTLV-1母子感染対策協議会が設置されているのは38都道府県であることがわかりました。WHOはHTLV-1感染対策に取り組んでいますか
WHOによる現在の感染予防対策はGlobal Health Sector Strategies on HIV, Viral Hepatitis and Sexually Transmitted Infectionsとして推進されており、ここではHTLV-1感染予防対策が性感染症対策の中に含まれています。このようにWHOも、HTLV-1をグローバルヘルスの観点において対策の必要性が高い重要な感染症であると位置づけており、その対策に取り組んでいます。
WHO HTLV-1テクニカルレポート
節外性NK/T細胞リンパ腫,鼻型
(extranodal NK/T-cell lymphoma, nasal type:ENKL)
総論
WHO分類(2017)ではNK細胞腫瘍として,節外性NK/T細胞リンパ腫,鼻型(extranodal NK/T-cell lymphoma,nasal type:ENKL),急速進行性NK細胞白血病(aggressive NK-cell leukemia:ANKL),慢性NK細胞リンパ増殖異常症(chronic lymphoproliferative disorders of NK cells:CLPD-NK)の3病型が記載されている1)。いずれも稀少病型であり,ANKLの頻度はENKLの7分の1以下であるため2),治療法に関するエビデンスは乏しい。このため本項ではENKLについてのみ取り扱う。
ENKLのほとんどはNK細胞由来であり,鼻腔およびその周辺(以下本項では鼻腔周辺)原発例においてT細胞由来のリンパ腫が少数存在するとされている。パラフィン材料を用いた現在の病理組織学的手法ではNK細胞型とT細胞型の鑑別ができないため,NK/Tとの用語が採用されている。NK細胞型とT細胞型の識別はフローサイトメトリーあるいはT細胞受容体再構成の遺伝子解析で可能となっており,鼻腔周辺以外の原発例およびANKLでは十分な検体が採取可能であるため識別できることが多い。鼻腔周辺原発例ではCD56発現に加えてEBウイルスの存在や細胞傷害性分子(TIA,Granzymeなど)の存在で他のPTCLとの鑑別を行っているのが現状である。
病期分類には,他の悪性リンパ腫と同様にLugano分類が用いられる。近年,アントラサイクリン非含有化学療法レジメンおよび治癒指向性放射線治療を受けた症例において樹立された予後予測モデルが提唱されている(PINK,PINK-E)3)。
PINK 4つの因子(年齢>60歳,Stage Ⅲ期またはⅣ期,遠隔リンパ節病変あり*,鼻腔外原発)
*鼻型の場合に腋窩リンパ節,鎖骨下リンパ節,縦隔リンパ節病変を有する。
PINKは予後因子の数によって以下の3つのリスクグループに分類する。
予後因子数0:低リスク
予後因子数1:中間リスク
予後因子数2~4:高リスク
PINK-E PINKの4つの因子(年齢>60歳,Stage Ⅲ期またはⅣ期,遠隔リンパ節病変あり,鼻腔外原発)に加えて,検出可能なEBV-DNAにつき各1点で計算する。
予後因子数0~1:低リスク
予後因子数2:中間リスク
予後因子数3~5:高リスク
臨床病期は治療法の選択に重要である。治療効果の判定に際しては,特に鼻腔周辺は解剖学的に複雑であること,腫瘍が消失しても粘膜肥厚などの非腫瘍組織の残存があり得ること,ENKLではpositron emission tomography(PET)検査において高率に18fluoro-2-deoxyglucose(FDG)の取り込みが認められることから4),FDG-PET/CTが有用である。
参考文献
1) Chan JKC, et al. Extranodal NK/T-cell lymphoma, nasal type. Swerdlow SH, et al. eds. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon, IARC; 2017: pp368-71.
2) Suzuki R, et al. Prognostic factors for mature natural killer(NK)-cell neoplasms: aggressive NK-cell leukemia and extranodal NK-cell lymphoma, nasal-type. Ann Oncol. 2010; 21(5): 1032-40.(3iiA)
3) Kim SJ, et al. A prognostic index for natural killer cell lymphoma after non-anthracycline-based treatment: a multicentre, retrospective analysis. Lancet Oncol. 2016; 17(3): 389-400.(3iiA)
4) Kako S, et al. FDG-PET in T-cell and NK-cell neoplasms. Ann Oncol. 2007; 18(10): 1685-90.
アルゴリズム
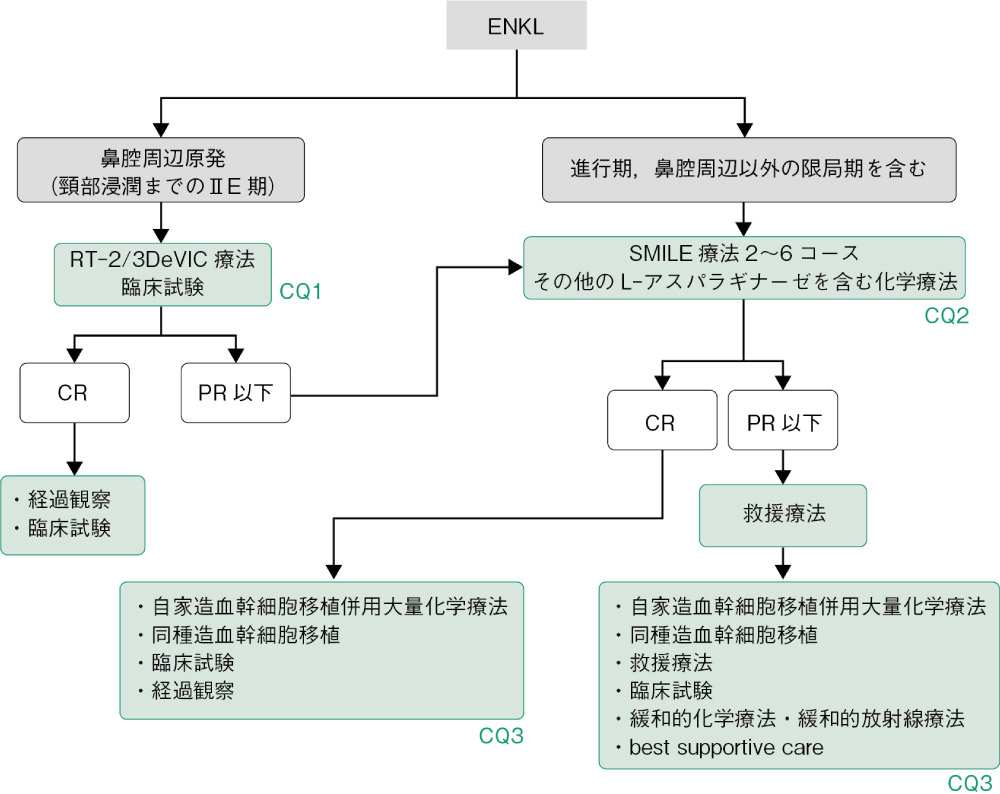
ENKLでは約7割の患者が鼻腔あるいはその周辺組織を中心とする限局期病変を有する。鼻腔周辺原発例で病変が頸部リンパ節までにとどまっている患者では,わが国で実施された第Ⅰ/Ⅱ相試験の結果から同時化学放射線療法であるRT-2/3DeVIC療法(DEX,ETP,IFM,CBDCA)を行うことが推奨され,また臨床試験への参加も勧められる(CQ1)。RT-2/3DeVIC療法で完全奏効(CR)を得た場合,地固め療法としての自家造血幹細胞移植併用大量化学療法(high-dose chemotherapy with autologous hematopoietic stem cell transplantation:HDC/AHSCT)を行うことは推奨されない。
鼻腔周辺原発で病変が腋窩リンパ節や縦隔病変など頸部リンパ節を超えて広がっている場合,鼻腔など上気道以外での発生例,初回治療後再発または部分奏効(PR)以下のENKLに対しては,第Ⅱ相試験の結果からSMILE療法(DEX,MTX,IFM,L-Asp,ETP)を行うことが推奨される(CQ2)。
初発進行期ENKLの全例および初回再発/治療抵抗性ENKLで救援療法後CR例では,エビデンスレベルは低いものの,移植後長期奏効を得ている患者が存在することから,年齢や全身状態などの問題がなければ,自家または同種移植が推奨される(CQ3)。救援療法によるPR以下のENKLの予後は不良であり,年齢や全身状態などの問題がなければ,自家または同種造血幹細胞移植が推奨される。
CQ1 初発鼻腔周辺限局期(頸部リンパ節浸潤までのⅡE期)ENKLに対してどのような治療が勧められるか
- 推奨グレード
- カテゴリー2A
同時化学放射線療法であるRT-2/3DeVIC療法が最も推奨される。ただし最良の治療法についてはコンセンサスがなく,臨床試験への参加も推奨される。
解説
ENKL患者の約7割が鼻腔あるいはその周辺組織を中心とする限局期病変を有する。ENKLではP糖蛋白関連薬を主体とするCHOP療法(CPA,DXR,VCR,PSL)の有効性が低く,この理由として正常NK細胞が多剤耐性(multi-drug resistance:MDR)に関与するP糖蛋白を発現していることが関連していると考えられている。一方で,病変部放射線治療単独により比較的良好なCR割合(65%)が得られることが早くから知られており1),放射線治療とMDR非関連薬を中心とする化学療法の併用療法が検討されてきた。多数例での後方視的解析において,アントラサイクリン含有化学療法に対するアントラサイクリン非含有化学療法の有効性と放射線療法併用の有効性が示されている2)。
稀少疾患であり,ランダム化比較試験により確立された標準治療はない。国内では,鼻腔周辺原発で病変が頸部リンパ節までの限局期ENKLを対象とし,同時化学放射線療法であるRT-2/3DeVIC療法(DEX,ETP,IFM,CBDCA)の第Ⅰ/Ⅱ相試験(JCOG0211-DI)が行われ3),OSが放射線治療単独の治療成績を上回り4),日常診療でも臨床試験と同様の効果および毒性であることが確認された5)。RT-2/3DeVIC療法のほかに臨床試験で開発されたものとしては,韓国の研究グループによるCCRT(RT,CDDP)-VIDL(ETP,IFM,DEX,L-Asp)療法6)などがある。RT-2/3DeVIC療法と比較して,CCRT-VIDL療法は治療期間が長いものの,放射線療法の線量は40Gyと低く抑えられている。最良の治療についてはコンセンサスがないものの,本邦において日常診療での安全性と有効性が確認されていることから5),RT-2/3DeVIC療法が最も推奨される。ただし,治療法の優劣は不明であり,臨床試験への参加も推奨される。臓器機能が保たれていないなど化学療法の同時併用もしくは追加を行えない場合は,放射線治療単独もオプションの一つとなり得る。
鼻腔周辺原発で病変が鎖骨下リンパ節など頸部リンパ節領域を超えて認められる場合は,放射線治療による有害反応が懸念されることに加え,限局期に対する治療では予後不良であることから5),進行期に準じて化学療法を行う。
初発鼻腔周辺限局期ENKLにおいて,初回治療後CRにおける地固め療法としてのHDC/AHSCTの有用性について,十分なサンプルサイズで評価した研究は少ない7,8)。さらに,MDR克服を意図した化学療法,あるいはそれらの併用による同時化学放射線療法を受けた患者を対象とした同様の研究はほとんどない。JCOG0211-DI試験では,治療後CR例ではHDC/AHSCTなどの後治療を行わず経過観察とされていた。また,国内31施設で日常診療としてRT-2/3DeVIC療法を受けたENKL患者150例の後方視的研究では,初回治療後CRでHDC/AHSCTを受けたのはわずか2例であり,そのうち1例で照射体積内の二次がん発生を認めた5)。5年OSはJCOG0211-DI試験で70%,後方視的研究で72%と良好であった。
以上より,RT-2/3DeVIC療法でCRとなれば,地固め療法としてのHDC/AHSCTを行わずに経過観察することが推奨される。米国造血細胞移植学会(ASBMT)の推奨ガイドでは,初回CR後HDC/AHSCTは実施すべきでないとされている9)。
参考文献
1) Kim GE, et al. Angiocentric lymphoma of the head and neck: patterns of systemic failure after radiation treatment. J Clin Oncol. 2000; 18(1): 54-63.(3iiA)
2) Qi SN et al. First-line non-antracycline-based chemotherapy for extranodal nasal-type NK/T-cell lymphoma: a retrospective analysis from the CLCG. Blood Adv. 2020; 4(13): 3141-53.
3) Yamaguchi M, et al. Phase I/II study of concurrent chemoradiotherapy for localized nasal natural killer/T-cell lymphoma: Japan Clinical Oncology Group Study JCOG0211. J Clin Oncol. 2009; 27(33): 5594-600.(3iiiA)
4) Yamaguchi M, et al. Concurrent chemoradiotherapy for localized nasal natural killer/T-cell lymphoma: an updated analysis of the Japan Clinical Oncology Group Study JCOG0211. J Clin Oncol. 2012; 30(32): 4044-6.(Correspondence)(3iiiA)
5) Yamaguchi M, et al. Treatments and Outcomes of Patients With Extranodal Natural Killer/T-Cell Lymphoma Diagnosed Between 2000 and 2013 : A Cooperative Study in Japan. J Clin Oncol. 2017; 35(1): 32-9.(3iiA)
6) Kim SJ, et al. Concurrent chemoradiotherapy followed by L-asparaginase-containing chemotherapy, VIDL, for localized nasal extranodal NK/T cell lymphoma: CISL08-01 phase II study. Ann Hematol. 2014; 93(11): 1895-901.(3iiiDiv)
7) Kim HJ, et al. High-dose chemotherapy with autologous stem cell transplantation in extranodal NK/T-cell lymphoma: a retrospective comparison with non-transplantation cases. Bone Marrow Transplant. 2006; 37(9): 819-24.(3iiA)
8) Lee J, et al. Autologous hematopoietic stem cell transplantation in extranodal natural killer/T cell lymphoma: a multinational, multicenter, matched controlled study. Biol Blood Marrow Transplant. 2008; 14(12): 1356-64.(3iiA)
9) Kharfan-Dabaja MA, at al. Clinical Practice Recommendations on Indication and Timing of Hematopoietic Cell Transplantation in Mature T-cell and NK/T-Cell Lymphomas: An International Collaborative Effort on Behalf of the Guidelines Committee of the American Society for Blood and Marrow Transplantation. Biol Blood Marrow Transplant. 2017; 23(11): 1826-38.(ガイドライン)
CQ2 鼻腔周辺以外の限局期,初発進行期および初回再発/治療抵抗性ENKL に対してどのような治療が勧められるか
- 推奨グレード
- カテゴリー2A
多剤併用化学療法であるSMILE療法が最も推奨される。
解説
初発ENKLでは,約25%が骨髄浸潤などの全身播種を示し,アントラサイクリンを含む化学療法が行われていた時代のCR割合は15%,50%生存期間は4カ月と極めて予後不良であった1)。多剤耐性(MDR)に関与するP糖蛋白の影響を受けない薬剤を主体とするSMILE療法(DEX,MTX,IFM,L-Asp,ETP)がわが国を中心として東アジアで開発され,年齢15~69歳,PS 0~2の初発Ⅳ期,初回治療後再発/治療抵抗性ENKLを対象として第Ⅱ相試験が行われ,既存の治療成績と比較して優れたCR割合,1年OSを示した2)。本試験は初期に感染症死が2例発生し,その後リンパ球数500個/μL以上を適格基準としたことには留意すべきである。
NCCNガイドラインでは初発例に対しペグアスパルガーゼを用いたSMILE療法変法や,オキサリプラチンを含むレジメン,再発難治例に対しては望ましいレジメンとしてペムブロリズマブとニボルマブを挙げているが,本邦では使用できない。
GELA/GOELAMSによる初回再発/治療抵抗性ENKLを対象としたAspaMetDex療法(L-Asp,MTX,DEX)の第Ⅱ相試験の結果が報告されているが,対象19例中12例が限局期例であり,17例は初回治療にCHOPまたはCHOP類似療法を受けていた3)。日本の初回標準治療を受けていた場合に,予後良好な患者が含まれている可能性がある。初発進行期例に対するAspaMet-Dex療法の第Ⅱ相試験も実施されたが,測定した全例で抗アスパラギナーゼ抗体が生じ,全奏効割合は58%にとどまった4)。このため,いずれの状態でも,現時点ではSMILE療法が最も推奨される。
参考文献
1) Suzuki R, et al. Prognostic factors for mature natural killer(NK)-cell neoplasms: aggressive NK-cell leukemia and extranodal NK-cell lymphoma, nasal-type. Ann Oncol. 2010; 21(5): 1032-40.(3iiA)
2) Yamaguchi M, et al. Phase II study of SMILE chemotherapy for newly diagnosed stage IV, relapsed, or refractory extranodal natural killer(NK)/T-cell lymphoma, nasal type: the NK-Cell Tumor Study Group study. J Clin Oncol. 2011; 29(33): 4410-6.(3iiiDiv)
3) Jaccard A, et al. Efficacy of L-asparaginase with methotrexate and dexamethasone (AspaMetDex regimen)in patients with refractory or relapsing extranodal NK/T-cell lymphoma, a phase 2 study. Blood. 2011; 117(6): 1834-9.(3iiiDiv)
4) Jaccard A, et al. A prospective phase II trial of an L-asparaginase containing regimen in extranodal NK/ T-cell lymphoma. Hematol Oncol. 2013; 31(Supple. S1): 129,[Abstract #099].(3iiiDiv)
CQ3 初発進行期ENKLおよび初回再発/治療抵抗性ENKLに対する救援療法による寛解導入後,地固め療法として造血幹細胞移植は勧められるか
- 推奨グレード
- カテゴリー2B
年齢や全身状態などの問題がなければ,自家または同種造血幹細胞移植が推奨される。
解説
予後不良とされてきた初回進行期および初回再発/治療抵抗性ENKLでは,これまで造血幹細胞移植療法なしに長期生存は困難であった。後方視的解析の結果ではあるが,自家移植1,2)もしくは同種移植3,4)を受けた一部患者で長期生存が報告されている。初発進行期ENKLを対象にVIDL療法(ETP,IFM,DEX,L-Asp)4コース後にupfrontの自家移植を併用した第Ⅱ相試験が報告され,27例中17例が自家移植を実施し,観察期間中央値31.2カ月において,PFS中央値は13.2カ月,OS中央値は27カ月,奏効期間中央値15.2カ月であった5)。なお,本試験では自家移植を実施した17例中4例で中枢神経再発をきたしている。近年レジストリ研究においてupfrontに自家移植が受けられた例での良好なPFSが報告された6)。
初発進行期ENKLおよび初回再発/治療抵抗性ENKLに対してSMILE療法(DEX,MTX,IFM,L-Asp,ETP)などL-アスパラギナーゼ(L-Asp)含有化学療法が行われている(CQ2)が,報告された臨床試験の成績は造血幹細胞移植が実施された患者を多く含むものである(2コースのSMILE療法完遂28例中19例に実施)4)。選択バイアスの可能性もあるが,サブグループ解析では自家または同種移植を受けた患者の方がOSは良好であった。化学療法のみで長期生存ないし奏効持続が得られるというデータはなく,現時点ではエビデンスレベルとしては低いが,患者の年齢や全身状態が問題なければ,自家または同種移植の実施が推奨される。
移植の種類に関しても選択バイアスの可能性はあるが,自家移植の成績は同種移植と同等かそれ以上であり2,7,8),CRで遂行可能な患者には自家移植実施の妥当性が示唆される。特に適切な同種骨髄・末梢血ドナーが存在しない場合,ドナー検索に時間をかけるより,CRでの自家移植の実施が推奨される。米国造血細胞移植学会(ASBMT)の推奨ガイドでは,自家移植はstrong recommendation,同種移植はweak recommendationとされているが,これを支持するエビデンスはない9)。
2024年11月1日 | カテゴリー:白血球異常 白血病・骨髄異形成症候群, リンパ節異常・リンパ球異常 |