ベネトクラクス +アザシチジンについて
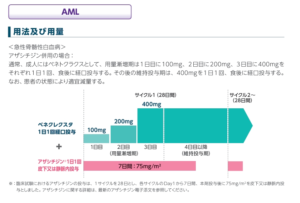
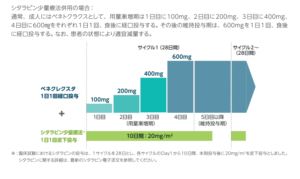
シタラビン誘導体であるアザシチジンは脱メチル化作用を有する抗腫瘍薬で,本邦において2011年にMDSに対する治療薬として承認,発売されました。ベネトクラクスは抗アポトーシス蛋白Bcl-2阻害薬で,2019年慢性リンパ性白血病に対して承認,発売されました。その後AMLに対して,アザシチジンでは臨床試験AZA-AML- 0011),ベネトクラクスではアザシチジンとの併用試験VIALE-A2),少量シタラビンとの併用試験VI ALE-Cが行われました3)。それら臨床試験の結果に基づきアザシチジンとベネトクラクスは2021年3月23日同日にAMLに適応を追加取得しました。
VIALE-A試験では,強力な寛解導入療法が適応とならない初発AML患者(75歳以上,あるいは心・肝・腎・肺機能低下)を対象にベネトクラクス(400mg/日)+アザシチジン(75mg/m2 7日間)(28日ごと)とアザシチジン単独(75mg/m2 7日間)(28日ごと)が比較検討されました。併用群での複合寛解率(完全寛解+末梢血回復の不十分な寛解)と全生存期間中央値は66.4%,14.7カ月,アザシチジン単独群ではそれぞれ28.3%,9.6カ月でした。
一部の高リスク骨髄性血液腫瘍において、新規経口薬ベネトクラクス(販売名:ベネクレクスタ)を標準治療に追加することについて安全性が認められ、また、初期の研究では、同剤との併用により、転帰改善が有望であることが示されていると、ダナファーバーがん研究所の研究者は述べている。
ベネトクラクスはがんの生存因子を標的としており、がん細胞を自滅させる治療に対してがん細胞を脆弱にさせる。同剤は、BCL-2阻害薬と呼ばれる新しい種類の最初の薬剤であり、2016年に慢性リンパ性白血病患者の一部を対象に初めて承認された。
第62回米国血液学会(ASH)年次総会において、ダナファーバーのJacqueline Garcia医師は、急性骨髄性白血病(AML)や骨髄異形成症候群(MDS)などの骨髄性血液腫瘍を有する高リスクの患者を対象に、ベネトクラクスと標準治療との併用の安全性と有効性を検討した2つの試験について報告した。
◇ 1つ目の試験では、急性骨髄性白血病(AML)または骨髄異形成症候群(MDS)患者を対象に、強度減弱前処置を用いた幹細胞移植の前に行う標準的な化学療法にベネトクラクスを追加した。強度減弱前処置を用いた移植は毒性が少ないため、高齢患者や併存疾患を有する患者に対して一般的に推奨されている。強度減弱前処置化学療法は、患者(レシピエント)の免疫系を低下させ、ドナー幹細胞(移植片)への拒絶反応を防ぐ目的で行われる。しかし、強度減弱前処置化学療法は、疾患再発のリスクが高いことに関連する。移植後に再発する骨髄性血液腫瘍患者では転帰が悪いため、試験責任医師らは、患者が移植を受ける前にAML細胞またはMDS細胞を殺すように計画された化学療法にベネトクラクスを加えて、造血系と免疫系を回復させることを発案した。これにより、フルダラビンとブスルファンからなる移植前化学療法が一層効果的になり、再発のリスクが軽減されることが期待された。
この戦略の有効性と安全性を検証するため、25歳から71歳までのAML、MDS、またはMDS/骨髄増殖性腫瘍(MPN)を有する患者22人にベネトクラクスを併用した。これらの患者のうち、35%が中間リスク群、65%が予後不良群であった。
Garcia医師らは、22人の患者全員にドナー細胞を移植した(移植後に細胞数が回復した)が、ベネトクラクスの追加投与による重篤な毒性は認められなかったと報告している。さらに、移植片対宿主病(GVHD)が生じた割合も、ベネトクラクスの追加投与による増加は認められなかった。この解析時点では、22人の患者のうち7人が再発し、そのうち5人が死亡していた。生存患者の生存率は中央値には達していないが、この集団の6カ月全生存率は84%、無増悪生存率は76%である。総合的に、非常にリスクの高い患者集団にしては心強い結果となった。
Garcia医師は、ベネトクラクスを追加しても毒性の増加は見られなかったと述べている。ベネトクラクス、フルダラビン、ブスルファンの併用療法は、「高リスクの疾患に対してさらなる評価を行うことを支持する有望な臨床効果であることを示している」とも述べている。
◇ Garcia医師が報告した2つ目の試験では、試験開始時に、治療を必要とするが、移植は直ちには実施しない高リスクの骨髄異形成症候群(MDS)患者に対して、ベネトクラクスとアザシチジンを併用投与した。アザシチジンは、DNAメチル化抑制剤として知られており、腫瘍抑制遺伝子の発現を増加させてがん細胞の増殖を遅らせる薬剤である。しかし、アザシチジン単独ではMDSの全奏効率は低く、全生存期間の中央値は約15カ月となっている。
研究者らによると、ベネトクラクスとDNAメチル化抑制剤との相乗効果が基礎研究では示されているという。この併用療法は、強化化学療法の適応がない未治療のAML患者の治療薬として、最近FDAに承認されている。ヒトでの安全性と有効性を検証するため、治療歴のない高リスクMDS患者57人にこの併用療法を実施した。患者の年齢は26~85歳で、中央値は71歳であった。
結果は、完全寛解42%、骨髄寛解42%を含む、全奏効率77%という顕著な結果であった。全生存期間中央値は未到達、効果持続期間中央値は14.8カ月であった。無増悪生存期間中央値は17.5ヵ月であった。
MDS患者は、基礎疾患による疲労やQOL低下を訴えることが多い。本試験では、治療中に患者から報告された治療効果についても評価が行われた。研究者らによると、身体機能は48週間の治療期間中も維持されており、治療に対する忍容性が確認されたという。さらに、疲労と息切れは第5サイクルを開始するまでに臨床的に意義のある改善が得られ、48週目まで維持された。
最もよくみられた有害事象は、便秘、好中球減少症、嘔気であった。最もよくみられた重篤な有害事象は、発熱を伴う好中球減少症で、その割合は42%であった。合併症を減らすため、予防的抗生物質の投与が必要とされた。
Garcia医師らは、ベネトクラクスとアザシチジンの併用療法は、「高リスクMDS患者に対して、効果持続性を含む有望な有効性と許容できる安全性プロファイルを示している」と結論付けた。これらの有望なデータに基づき、高リスクMDSに対する初回治療において、アザシチジン+ベネトクラクスとアザシチジン+プラセボを比較する第3相臨床試験(VERONA)が開始された。
Garcia医師は、Eli Lily、Pfizer、Genentech、AbbVieから研究資金を受けていることや、AbbVieのコンサルタントの任務についていることなどを公表している。
The prognosis of adult acute myeloid leukemia (AML) remains poor, with the long-term survival rate less than 50%. However, the current paradigms of treatment are changing through a better understanding of the disease genetics and pathophysiology. Since 2017, eight new drugs have been approved by the U.S. Food and Drug Administration for the treatment of AML, including the FLT3 inhibitors midostaurin and gilteritinib, the IDH inhibitors ivosidenib and enasidenib, the anti-CD33 monoclonal antibody gemtuzumab ozogamicin, liposomal daunorubicin and cytarabine, the hedgehog pathway inhibitor glasdegib and the BCL-2 inhibitor venetoclax. Preclinical data demonstrated the anti-leukemic efficacy of venetoclax in AML and its synergy when combined with hypomethylating agents or chemotherapy agents. Clinical trials have demonstrated the clinical benefit of venetoclax-based therapies in newly diagnosed AML, leading to the recent FDA approval of venetoclax in combination with hypomethylating agents or low-dose cytarabine for older adults with newly diagnosed AML. Herein, we focus on the role of single-agent BCL-2 inhibition in AML and review the clinical studies of venetoclax-based combination regimens and the evolving mechanisms of resistance.

venetoclax pdbqt 像
2024年9月18日 | カテゴリー:各種治療学, 白血球異常 白血病・骨髄異形成症候群 |