乳がん治療法の細分化が進む理由
「従来のサブタイプは、乳がんの生物学的特性を表しています。例えば、ホルモン受容体陽性、HER2陰性で、がんの顔つきが悪い(Ki67数値が高値)などのがん細胞の性質を調べ、それに応じて治療法が決まっていました。そこに新しい薬剤が次々に登場したため、PD-L1抗体やBRCA病的バリアントの有無を調べ、陽性なら新しい治療薬が使用できるという形で治療法の細分化が進んできたのです。PD-L1やBRCA遺伝子変異の有無を見ることは、がんの性質だけでなく、その人が生まれ持つ遺伝子なども見ています。そして、新しく承認された薬剤による効果が期待できるか否かを判断しているのです。乳がんの生物学的タイプが枝分かれしたとか、増えたという意味ではありません」と、がん研有明病院乳腺センターは説明します。
さらに2023年3月には、進行・再発乳がんのHER2低発現(HER2-low)に対して、2次治療以降で抗体薬物複合体(ADC)エンハーツ(一般名トラスツズマブ デルクステカン:T-DXd)が使えるようになったことを受け、HER2低発現か否かも治療選択に関わるようになりました。
HER2は発現度合いによって、HER2(0)(1+)(2+)(3+)の4段階に分けられますが、これまでは(3+)のみがHER2陽性、それ以外はHER2陰性と分類されていました。しかし、実際は(1+)(2+)はHER2が全く発現していないのではなく、低発現なのです。つまり、これまでHER2陰性だった(1+)と(2+)はHER2低発現と分類され、エンハーツが使用できるようになったのです。
こうしたことを踏まえ、2023年現在、最新の乳がん薬物療法選択の指針図に示しました(図3)。
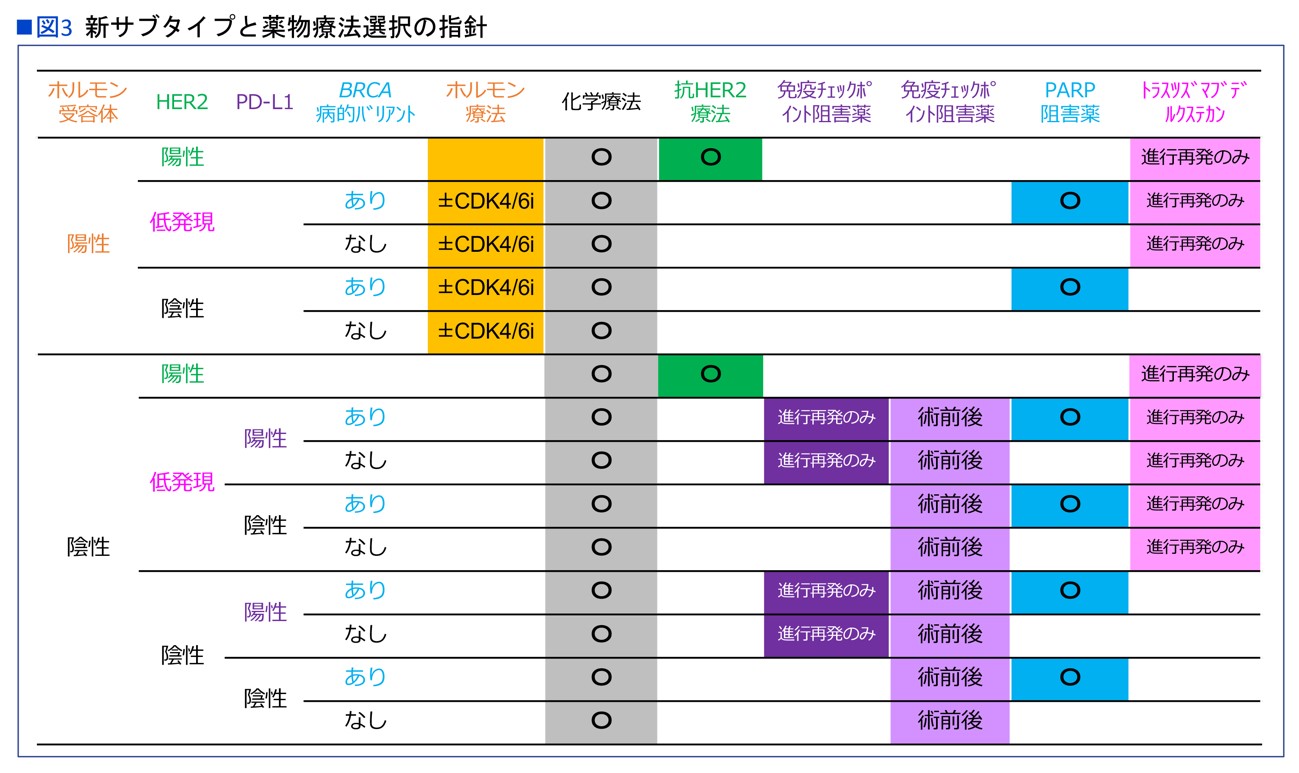
〝私の乳がんはどの薬剤に効果が期待できるのだろう〟と考えるとき、図3の横軸を見ます。たとえば〝ホルモン陰性、HER2低発現、PD-L1陽性、BRCA遺伝子変異陽性〟ならば、上から7段目に当たります。
化学療法はすべてのケースに適応します。生物学的特性よるタイプ分類では、HER2低発現はHER2陰性に入るので、このケースはトリプルネガティブと評価され、PD-L1やBRCAも検査されなかった数年前までは、化学療法しか方法がありませんでした。
ところが現在、PD-L1陽性にはキイトルーダ(一般名ペムブロリズマブ)、BRCA陽性にはPARP阻害薬リムパーザ(同オラパリブ)、そしてHER2低発現にエンハーツが加わり、効果を期待できる薬剤がいっきに増えたのです
新薬が次々登場している乳がん治療は今、がんの生物学的特性による分類だけでなく、新しい薬剤の効果が期待できるかどうかで治療法を選択する時代になったと言えるでしょう。
手術前後(周術期)の薬物療法
まずは切除可能な乳がんにおける、手術前後の薬物療法について具体的に見ていきます。
ホルモン受容体陽性、HER2陰性の場合(ルミナル型)
女性ホルモンががんの餌になっている、いわゆるルミナル型といわれるタイプです。このタイプには、ホルモン療法が基本で、抗がん薬を追加すべきか否かがポイントとなります。リンパ節転移が複数(4個以上)、がんの径5㎝以上など、明らかに高リスクと判断される場合は、手術前に多くは抗がん薬治療を行います(術前化学療法)。
Ⅰ期は術後の抗がん薬が不要の可能性があるので、まず手術を行い、術後に病理検査と、場合によってはオンコタイプDX(2023年9月1日保険適用)で抗がん薬を投与すべきかを判定します。
リンパ節転移の有無や病理検査などで低リスクと判定された場合は、術後、ホルモン療法のみです。また、BRCA陽性に使えるPARP阻害薬リムパーザは高リスクにのみ適応のため、低リスクの場合は、BRCA遺伝子変異の有無は調べません。
ただ、BRCAを調べる理由は実は2つあって、1つはリムパーザを使えるかどうかの判定のため。もう1つは家族的遺伝性の有無を知るため。前者の場合は高リスク時しか調べませんが、後者の場合は、どのタイプにせよ低リスクでも調べることがあります
2022年の乳癌診療ガイドライン改訂で、周術期のホルモン受容体陽性、HER2陰性の高リスクに対して、ホルモン療法に分子標的薬CDK4/6阻害薬ベージニオ(一般名アベマシクリブ)を2年間併用することが強く推奨されました。さらに、中間リスクと高リスクに対し、TS-1(一般名S-1)を1年間併用することも強く推奨されたのです。
これにより、リンパ節転移4個以上の場合はホルモン療法にベージニオを併用し、リンパ節転移1~3個の場合はがんが5㎝以上、もしくは悪性度3なら高リスクに分類されるので、同じくベージニオを併用します。一方、リンパ節転移1~3個で5㎝未満、および悪性度3未満の場合は中間リスクとなり、TS-1を併用します。TS-1は高リスクでも使えますが、高リスクの場合はベージニオを使うほうが多いようです
使用するタイミングとしては、CDK4/6阻害薬はホルモン療法を助ける機序を持つため、ホルモン療法と同時投与。
高リスクでBRCA陽性の場合、ホルモン療法+ベージニオとオラパリブ、どちらの治療法を先に選択するか。その順序にはエビデンスがないので、世界の専門家が集まるザンクトガレンなどのコンセンサス会議などで議論されます。BRCA陽性の場合はPARP阻害薬の効果が高いことがわかっているので、大半の専門家がオラパリブを先にすることに同意されていました
ホルモン陰性、HER2陽性の場合(HER2型)
低リスクのⅠ期なら、術後に抗HER2薬ハーセプチン(一般名トラスツズマブ)+タキソール(一般名パクリタキセル)の2剤のみ。Ⅱ期以降は、術前にハーセプチンだけでなく抗HER2薬パージェタ(同ペルツズマブ)も加えます。
パージェタを使う際には、その前に*EC療法、もしくは*AC療法を行い、さらにタキソテール(一般名ドセタキセル)に抗HER2抗体ハーセプチンとパージェタを組み合わせます。HER2陽性の場合は、Ⅱ期から高リスクと捉えます その後、手術。術後に病理学的寛解(pCR)を得られたら、引き続きハーセプチンとパージェタを続け、pCRが得られなかった場合は、ADCのカドサイラ(一般名トラスツズマブ エムタンシン:TDM-1)になります。
*EC療法:ファルモルビシン(一般名エピルビシン)+エンドキサン(同シクロフォスファミド)
*AC療法:アドリアシン(同ドキソルビシン)+エンドキサン
トリプルネガティブの場合
周術期の高リスクのトリプルネガティブに対して、昨年(2022年)9月、PD-L1の有無を問わず、術前術後に免疫チェックポイント阻害薬のキイトルーダ(一般名ペムブロリズマブ)が乳がんで初めて保険適用されました。
キイトルーダは、術前術後にまたがった臨床試験によって承認されたので、術前に使っていないと術後には使えません。術前には使わなかったけれど、術後にリンパ節転移があると診断され、その時点からキイトルーダを使用したいと思ってもできないそうです。最近の承認なので、術前にはキイトルーダを使いたくても使えなかったという悩ましいケースも存在するそうです。
また、ガイドライン改訂で、周術期、高リスクのBRCA陽性乳がんに対してオラパリブの有用性が示されたため、トリプルネガティブ高リスクの場合も、BRCA陽性ならばオラパリブを使用できるようになりました。
Ⅰ期の低リスクに関しては、従来通り、術後にアンスラサイクリン系+タキサン系抗がん薬の併用療法となります。
日本人の2人に1人が一生に1度はがんと診断される時代、中でも、女性の罹患者数がもっとも多いのが乳がんです。現在、日本人女性の9人に1人が乳がんと診断されています。
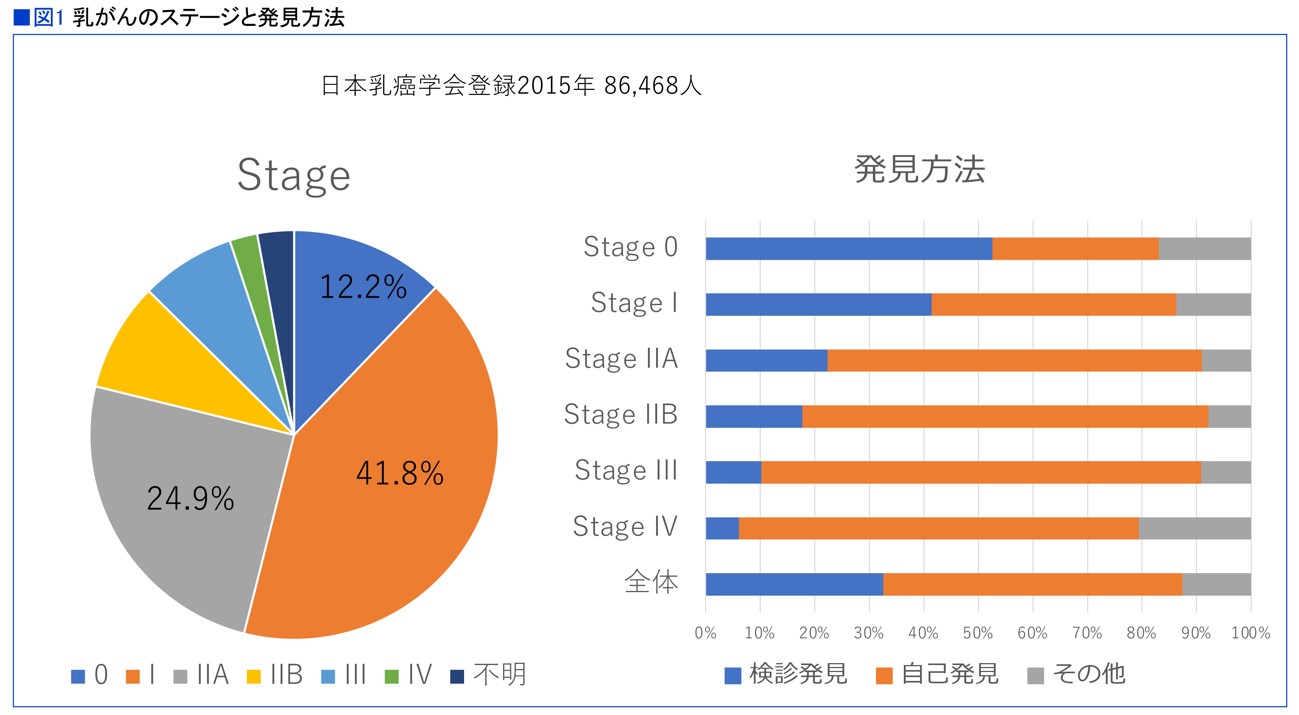
一方で、検診率上昇に伴って乳がんは早期発見が増えており、5割以上がⅠ期までで見つかるようになりました。現在、乳がん全体の5年生存率は92.2%、病期(ステージ)別では、0期100%、Ⅰ期では99.8%、Ⅱ期95.5%、Ⅲ期80.7%。乳がんは、治療しながら自身の人生を生きていける病気になっています。ただ、他臓器に遠隔転移しているⅣ期となると、5年生存率は現在も38.7%にとどまります(図1)。
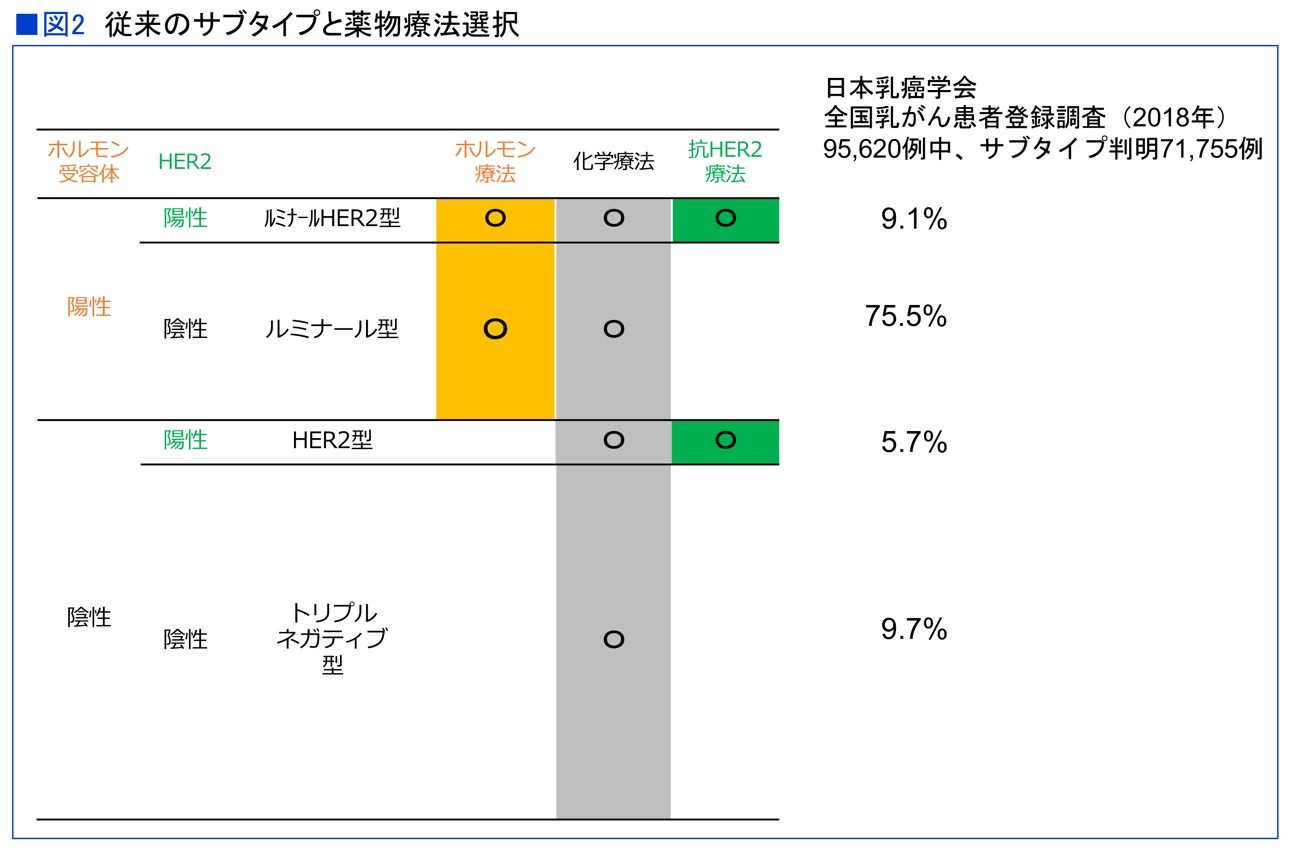
20年前は誰も〝サブタイプ〟を知りませんでしたが、今では患者さん自身が、ルミナル型などのサブタイプ分類の名称は知らなくても、自分の乳がんが「ホルモン受容体(HR)陽性でHER2は陰性」とか「トリプルネガティブ」といったことは把握し、タイプに応じた薬物療法が行われることを理解するようになっています(図2)。
2024年9月22日 | カテゴリー:各種治療学, 各種病因学, 癌の病態生理と治療学 |